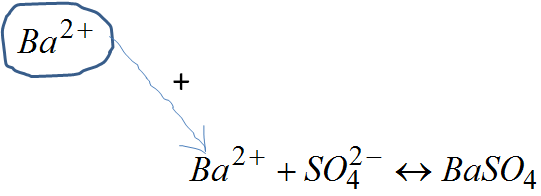Analiza Wagowa: Jak Ważenie Osadów Może Uratować Twój Dzień!
Analiza wagowa, czyli metoda dla tych, którzy chcą wiedzieć, co siedzi w środku jakiejś substancji, a przy okazji dobrze się bawić! To sposób na oznaczanie zawartości pierwiastków w różnych materiałach. Ale uwaga, nie wszystko można tu zważyć! Sprawdźmy, jak to działa!
Kiedy Analiza Wagowa Się Sprawdzi?
Metoda ta działa tylko wtedy, gdy pierwiastek tworzy taką sól, której nawet gorąca herbata nie rozpuści. :) Więc jeśli coś jest bardziej uparte, to analiza wagowa może być strzałem w dziesiątkę! Używamy jej do oznaczania rzeczy jak BaSO4 czy AgCl – i chociaż brzmi to jak szyfr, w chemii to klasyka.
Ciekawostka: W laboratoriach chemicznych ta metoda nie jest już tak popularna. Nie dlatego, że nie działa, ale dlatego, że trwa dłużej niż maraton serialowy!
Jak Przeprowadzić Analizę Wagową?
Prosta sprawa! Najpierw wywołujesz osad (czyli taką chemiczną wersję deszczu w szklance), potem go przemywasz, sączysz, suszysz, prażysz... tak, jakbyś przygotowywał idealne ciasteczka na imprezę. Kiedy masz osad o znanej masie – przeliczasz to na pierwiastek. I voila! Chemiczna magia działa!
3 Złote Zasady Analizy Wagowej, Które Uratują Cię Przed Klęską
1. Osad musi być super trudny do rozpuszczenia
No bo jak chcesz coś zważyć, jak to coś się rozpuszcza? Taka sól musi być twarda jak skała, a nie jak cukier w herbacie!
2. Osad musi przetrwać więcej niż ciepły wiatr
Wyobraź sobie, że wytrącasz osad, a ten znika przy pierwszej fali ciepła. No, nie ma takiej opcji! Musi być trwały i nie rozpadnie się nawet podczas suszenia czy prażenia – dosłownie chemiczny gladiator.
3. Osad powinien być grubokrystaliczny, jak diament
Żadne tam galaretki! Osady galaretowate to najgorsze, co może Cię spotkać. Takie Cu(OH)2 chwyta wszystko, co się da, i finalnie zaburza wynik. Do tego zapychają sączki, a czas pomiaru się wydłuża. Koszmar chemika!
Pro Tip: Jak Otrzymać Idealny Osad (I Przy Okazji Nie Zwariować)
- Strącaj powoli – jakbyś nalewał kawę do filiżanki. To wszystko po to, żeby układ miał czas na wytworzenie kryształów. Dodanie dużej ilości czynnika strącającego o dużym stężeniu powoduje wytrącenie osadów amorficznych, które są trudne do przemywania i sączenia.
- Dodaj odczynnik strącający z rozwagą – więcej w tym przypadku naprawdę znaczy lepiej! Reguła przekory chemicznej działa tu jak w życiu – im więcej, tym lepiej. Odczynnik strącający dodaje się w nadmiarze po to, żeby przesunąć równowagę reakcji w kierunku osadu. To powoduje jeszcze pełniejsze wytrącenie. Wynika z reguły przekory. Dodanie nadmiaru jonów baru przesuwa równowagę rekcji w kierunku produktów, czyli osadu.
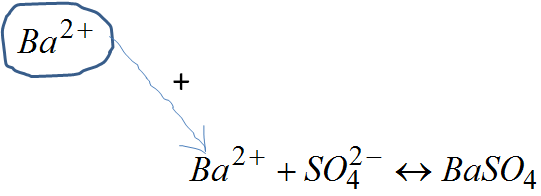
- Daj osadowi czas na wyrośnięcie – zostaw go w roztworze na kilka godzin, jakby to było ciasto na pizzę. A czasem warto go jeszcze podgrzać, bo ciepło działa cuda! Po strąceniu osadu należy go pozostawić w roztworze na kilka godzin w celu wzrostów kryształów. Czasami stosuje się metodę strącania osadów w ciepłym roztworze. Takie roztwory w niektórych przypadkach również sprzyjają wzrostowi kryształów.
Podsumowanie: Analiza Wagowa – Naukowa Cierpliwość i Precyzja!
Jeśli chcesz zgłębić tajniki analizy wagowej, albo musisz zaliczyć ten temat na studiach, zapraszam do mojego kursu chemii analitycznej! Dowiesz się, jak nie tylko strącać osady, ale też jak przejść przez studia z uśmiechem na twarzy (i może trochę szybciej niż trwa ta analiza wagowa). Kurs z chemii analitycznej
Nie zapomnij odwiedzić mojego facebooka , gdzie znajdziesz więcej chemicznych smaczków!