Praca objętościowa
Aby wyprowadzić wzór na pracę objętościową trzeba zacząć od wzoru ogólnego na pracę, jaki na pewno poznałeś w fizyce. Jeśli wymnożysz siłę razy przemieszczenie to otrzymasz pracę.
W=F*L
Wyprowadzę ten wzór korzystając z zapisu różniczkowego.
Nic się nie przejmuj, to tylko tak groźnie brzmi, natomiast idea jest bardzo prosta. Co się stanie jeśli siłę wymnożysz, ale razy bardz,o bardzo małe przemieszczenie (dużo mniejsze od przemieszczenia jakie planujesz wykonać)? Otrzymasz bardzo, bardzo małą pracę. W fizyce i matematyce do nieskończenie małych zmian (bardzo małych zmian) wykorzystuje się literkę „d”, dlatego zapis tej bardzo małej pracy musi wyglądać tak:
dW=F*dL
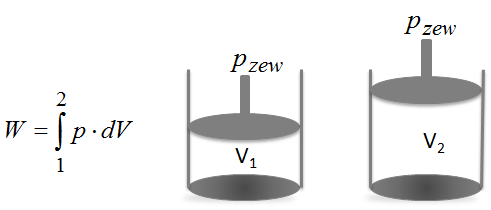
Jak zsumujemy wszystkie nieskończenie małe przemieszczenia to finalnie otrzymamy całkowitą pracę jaką wykonano na całym odcinku. Do sumowania nieskończenie małych zmian w matematyce wykorzystuje się całkę, dlatego zapis wzoru na pracę wygląda tak:
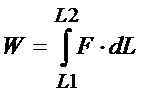
A teraz spróbujmy odnieść ten wzór na pracę do konkretnego przykładu, a mianowicie do obliczenia pracy objętościowej jaką wykona gaz zamknięty w cylindrze z ruchomym tłokiem.
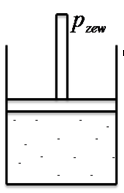
Ze względu na to, że w cylindrze mamy gaz to znacznie łatwiej byłoby operować ciśnieniami niż siłą, dlatego w kolejnym kroku postaramy się w miejsce siły podstawić ciśnienie. Zależność między ciśnieniem a siłą przedstawia się w następujący sposób:
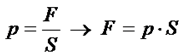
Następnie w miejsce siły wstawmy powyższą zależność:
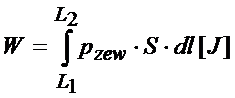
Wymnożenie pola powierzchni razy nieskończenie małe przemieszczenie daje nam nieskończenie małą objętość.
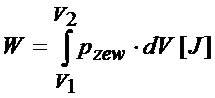
I teraz w zależności od książek wzór na tę pracę albo ma minus przed całką, albo go nie ma. Powiem szczerze mi ten temat spędzał sen z powiek przez całe studia, dodam, że wówczas w internecie jeszcze nie wiele można było znaleźć, więc siedziało się w czytelni całymi godzinami i przeglądało różne książki. W jednych książkach wzór na pracę objętościową był ze znakiem minus tak jak poniżej:
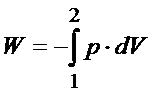
A w innych ze znakiem plus:
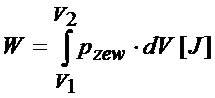
Pytanie jakie samo się nasuwa „kto ma rację” ? Który wzór jest poprawny? Uwzględniać ten minus czy nie?
Czas rozwiać te wątpliwości i wytłumaczyć w czym rzecz!
We wszystkich książkach z chemii fizycznej praca objętościową jest z minusem. Tak więc chemicy, wy nie musicie się zastanawiać! Dla was wzór na pracę objętościową zawsze jest z minusem!
Mechanicy teraz wy. W waszym przypadku sprawa się troszeczkę komplikuje. W zależności kto was uczy termodynamiki na studiach, raz wzór na pracę będzie z minusem, a innym razem z plusem. Skąd te rozbieżności? Jeśli termodynamikę będzie wam wykładał „rasowy mechanik” to dla niego praca prawdopodobnie będzie z plusem. Jeśli natomiast ten przedmiot wykłada wam ktoś z wydziału chemicznego to prawdopodobnie będzie wam mówił, że praca jest z minusem! Skąd te różnice?
Najpierw to co twierdzą chemicy fizyczni :)
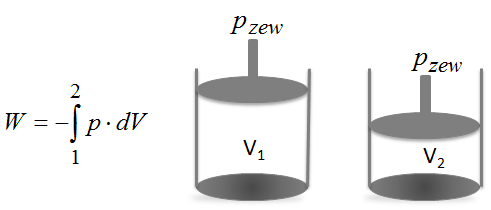
Chemicy uważają, że wynik dodatni z pracy musimy otrzymać wtedy, gdy otoczenie wykonuje pracę nad układem tzn. tłok ściska gaz wewnątrz cylindra, bo właśnie w takim przypadku energia wewnętrzna układu rośnie. Właśnie dlatego we wzorze na pracę jest minus, bo dzięki temu przy sprężaniu gazu wynik z pracy wychodzi dodatni.
Ujemną pracę otrzyma się, gdy to układ wykonuje pracę nad otoczeniem, czyli gaz w cylindrze się rozpręża, a wówczas energia wewnętrzna układu maleje.
Jak widzisz, dla chemika najważniejsza jest energia wewnętrzna układu. On patrzy na układ właśnie z tej strony i zastanawia się czy dana zmiana powoduje wzrost energii wewnętrznej gazu czy nie.
Teraz mechanicy
Mechanicy natomiast uważają, że wynik dodatki pracy musimy otrzymać wtedy, gdy to układ wykona pracę i przekaże ją do otoczenia, właśnie dlatego w ich wzorze na pracę nie mamy minusa. Z praktycznego punktu widzenia mechanika interesuje dużo mniej energia wewnętrzna układu. Jego interesuje to, aby gaz który jest w cylindrze rozprężył się, bo wówczas to spowoduje napędzanie układu.
Pracę ujemną otrzymujemy wtedy, gdy otoczenie wykonuje pracę nad układem (my musimy zużyć energię, żeby sprężyć gaz w tłoku).
W dalszym omówieniu wykorzystam wzór na pracę z minusem
- a) Procesy nieodwracalne: tak się nazywa proces, gdy na tłok działa cały czas takie same ciśnienie. Przykładem takiego procesu może być np. ciśnienie atmosferyczne, które w trakcie eksperymentu nie zmienia się. Jeśli więc ciśnienie się nie zmienia (jest stałe) to znaczy, że możemy wówczas ciśnienie wyrzucić przed znak całki (wszystkie stałe można wyrzucać przed znak całki).
Wówczas do scałkowania mamy następujące wyrażenie:
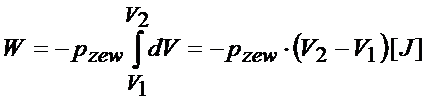
- b) Proces odwracalny: w procesie odwracalnym ciśnienie na zewnątrz tłoka i wewnątrz jest takie same. Gdy np. na zewnątrz tłoka ciśnienie nieznacznie wzrośnie to gaz w cylindrze zostanie bardziej ściśnięty tak, że ciśnienie w cylindrze się wyrówna z tym, które jest na zewnątrz. Takie nieskończenie małe zmiany są procesami odwracalnymi. Jeśli zachodzi taka zależność między ciśnieniem zewnętrznym i wewnętrznym to niestety, ale tym razem ciśnienie jest wartością stałą, nie można go wyrzucić przed znak całki. Jeśli ciśnienie jest zmienne to zgodnie z jaką funkcją się zmienia? Możliwości tutaj jest bardzo dużo, ale takie najbardziej popularne jest zastosowanie w tym miejscu równanie gazu doskonałego (równanie Clapeyrona), równanie sztywnych kul lub van der Waalsa. O tych równaniach mówiłem więcej w poprzednich artykułach
Jeśli założymy, że gaz zachowuje się jak gaz doskonały to ciśnienie można opisać właśnie za pomocą tej funkcji:
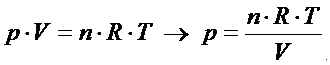
Teraz ciśnienie możemy podstawić do wzoru na pracę.
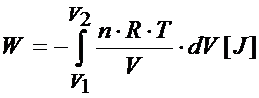
Liczba moli gazu w cylindrze się nie zmienia, stała gazowa też jest wielkością stałą, jeśli temperatura również się nie zmienia to ją również możemy wyrzucić przed znak całki. Pracę wówczas można obliczyć ze wzoru poniżej:
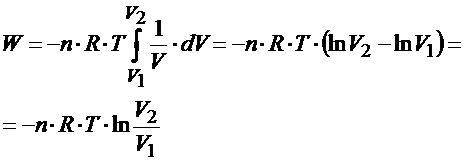
Jeśli tematyka Cię interesuje i szukasz zadań z chemii fizycznej, albo z termodynamiki to na naszej stronie internetowej mamy 2 kursy odnośnie tych tematów:
Chemia fizyczna 1a https://fizyka-kursy.pl/kurs/chemia-fizyczna-1a
Termodynamika 1a https://fizyka-kursy.pl/kurs/termodynamika-1a




