Entropia - Co To Jest i Jak Zmienia Nasz Świat (Plus Pajęczyny na Wakacjach)
Cześć! Gotowy na wesołą podróż w świat entropii? To nie będzie nudna lekcja fizyki, ale przygoda pełna śmiechu, kurzu i... pajęczyn! Bo entropia, mój drogi, otacza nas na każdym kroku. Nawet wtedy, gdy leżysz na plaży, a Twój dom powoli zamienia się w królestwo kurzu.
Entropia na Wakacjach – Czyli Skąd Te Pajęczyny?
Wyobraź sobie, że wyjeżdżasz na wymarzone wakacje. Powracasz, pełen energii i pozytywnej energii... a tam? Dom pełen kurzu, pajęczyn i ogólnego chaosu. Co się stało? Nikt przecież nie mieszkał! To nie Twoja wina, tylko entropii! Natura dąży do nieporządku, a II zasada termodynamiki mówi nam jasno: entropia zawsze rośnie (nieporządek zawsze rośnie)! W skrócie: dom sam się nie sprzątnie. Niebywałe, ale nieporządek również da się policzyc. Entropia jest miarą nieporządu.
Matematyka Entropii – Czyli Jak Policzyć Bałagan
Teraz troszkę naukowo, ale spokojnie – będzie wesoło! Entropię oznaczamy jako ΔS (tak, to ten dziwny symbol). Jeśli ΔS rośnie (ΔS>0), mamy do czynienia z bałaganem, którego nie da się odwrócić. Przykład? Proszę bardzo! Przepływ ciepła – zawsze z ciała gorącego do zimnego. Spróbuj odwrócić ten proces! Nie da rady? No właśnie, proces nieodwracalny jak kubek gorącej herbaty na zimowej stacji.
Przykłady Procesów Nieodwracalnych – Ciepło, Gorąco i Kawa
Okej, teraz coś prostszego: przepływ ciepła! Ciepło zawsze przechodzi z miejsca cieplejszego do chłodniejszego. Pomyśl o filiżance gorącej kawy, która po kilku minutach staje się zimna. Kto nie chciałby, żeby kawa zawsze była gorąca? Ale sorry, entropia mówi: "Nie ma takiej opcji!"
Procesy Odwracalne – Sprężyny, które Wracają
A co w przypadku procesów odwracalnych? Zmiana entropii takiego układu jest równa zero ΔS=0. Są jednak procesy, które można odwrócić. Przykład? Sprężyna! Możesz ją naciągnąć, a potem wróci do pierwotnej formy – jakby nigdy nic. To właśnie proces odwracalny, w którym entropia ΔS = 0. Nieporządek da się cofnąć, więc nasza kochana sprężyna wraca do stanu początkowego, a świat znowu jest w harmonii.
Jak Zmieniać Entropię? Produkcja vs Transport
Ale jak zmieniać entropię? To proste – mamy dwa sposoby. Po pierwsze, produkcja entropii. Kiedy np. zachodzi reakcja chemiczna, wydziela się ciepło, a wraz z nim chaos – i entropia rośnie. Po drugie, mamy transport entropii – dostarczamy coś do układu z zewnątrz, na przykład nowy kurz do Twojego pokoju.
W taki sposób można zmieniać entropię układu.

Procesy Odwracalne vs Nieodwracalne – Kiedy Entropia Rośnie?
W procesie odwracalnym gdy się zsumuje zmianę entropii układu i otoczenia to jest ona równa zero. Dodatkowo w takim układzie produkcja entropii jest równa zero a zmianę entropii można dokonać tylko na skutek transportu entropii.
Jeśli natomiast chodzi o procesy samorzutne i nieodwracalne to zmiana entropii układu i otoczenia zawsze jest większa od zera. Tak więc jeśli Ci wyjdzie, że suma zmian entropii jest większa od zera to znaczy, że masz do czynienia z procesami samorzutnymi i nieodwracalnymi.
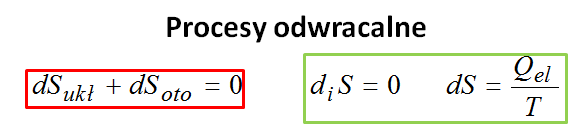

Transport Entropii – Jak Obliczyć Ten Chaos?
Jak obliczyć transport entropii? Potrzebujesz ciepło oraz temperaturę!
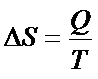
Jak Policzysz Entropię? Czas na Praktykę!
Entropię można obliczyć, dzieląc ciepło przez temperaturę.
Ciepło możesz znaleźć we wzorze na zmianę entalpii oraz w pierwszej zasadzie termodynamiki (zmiana energii wewnętrznej). Który z tych wzorów będziesz najczęściej wykorzystywał do obliczenia ciepła? Zdecydowanie najczęściej będziesz korzystał ze wzoru na zmianę entalpii. Dlaczego? A dlatego, że większość procesów odbywa się w stałym ciśnieniu, a jak mamy do czynienia ze stałym ciśnieniem to najlepiej skorzystać z entalpii, bo wówczas wzór nam się upraszcza (znika człon Vdp – patrz poniżej) i wychodzi, że ciepło jest równe zmianie entalpii.
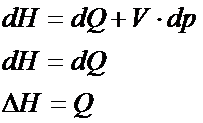
Do tej pory zmianę entalpii czy energii wewnętrznej można było obliczyć korzystając z różniczki zupełnej. W przypadku entropii jest tak samo. Również możemy skorzystać z różniczki zupełnej! Żeby więc napisać różniczkę zupełną dla entropii trzeba wiedzieć jakie parametry wpływają na nieporządek układu. Na pewno na nieporządek wpływa zmiana temperatury, ciśnienia i objętości. W związku z tym różniczkę zupełną dla entropii możemy napisać w 2 wersjach jak poniżej:

Zdecydowanie najczęściej do obliczenia zmiany entropii będziesz korzystał z tych 2 wzorów znajdujących się powyżej w czerwonej ramce.
Link do Kursu – Dowiedz Się Więcej
Żeby dobrze zrozumieć entropię, musisz trochę poćwiczyć. Sprawdź mój kurs z chemii fizycznej, w którym znajdziesz zadania i przykłady. Na pewno pomogą Ci lepiej ogarnąć ten temat. Powodzenia na kolokwiach!




